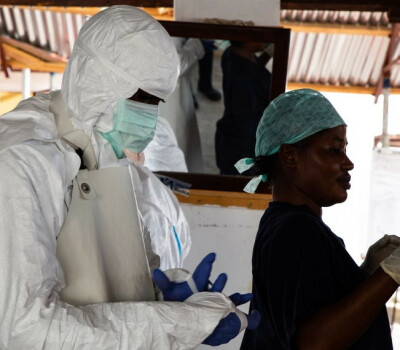
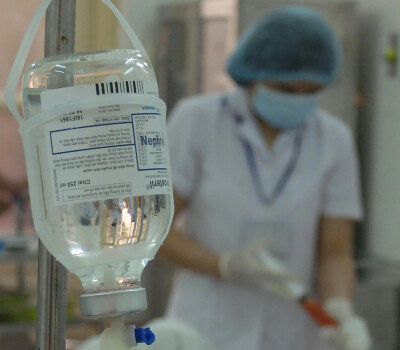
"AI geeft wetenschappers superkrachten, maar ook superverantwoordelijkheden"
Oren Tzfadia is senior onderzoeker in de Computationele Biologie bij de Dienst Biomedische Wetenschappen van het Instituut voor Tropische Geneeskunde (ITG) in Antwerpen. Hij is gedreven om te begrijpen hoe onze genen functioneren en gebruikt algoritmen en big data om nieuwe inzichten te ontdekken in de genetische processen daarachter. In het bijzonder gebruikt hij dat in het gevecht tegen geneesmiddelenresistente tuberculose, wereldwijd nog steeds een van de dodelijkste infectieziekten. Over dit thema spreekt hij binnenkort tijdens het ITG Colloquium.

We horen tegenwoordig veel over ‘omics’ in gezondheidsonderzoek. Wat zijn dat en waarom zijn ze zo belangrijk?
OREN TZFADIA: In plaats van één gen of één biologische route tegelijk te bestuderen, analyseren we het hele organisme. Die aanpak heet omics. Een gen is een stukje DNA dat informatie bevat om te worden vertaald naar RNA en vervolgens naar een specifiek eiwit. Die eiwitten sturen en regelen hoe het lichaam functioneert. Wanneer een gen muteert, kan dat de werking van het eiwit beïnvloeden. Genetisch onderzoek helpt bepalen welke genen ziektes veroorzaken en invloed hebben op het behandelingsresultaat.
Dankzij technologische vooruitgang kunnen we nu alle genen in kaart brengen (genoom), RNA-niveaus meten (transcriptoom) en alle eiwitten analyseren (proteoom). Zie het als het verschil tussen luisteren naar één muzikant of naar een volledig orkest: het geeft een veel completer samenspel van de biologische processen.
Omics is een sleutelbegrip geworden, nu we eindelijk de technologie en rekenkracht hebben om enorme datasets te genereren én analyseren. Door AI en geavanceerde informaticatools kunnen we multilagenonderzoek uitvoeren: dat transformeert de biomedische wetenschap. Het opent de deur naar ontdekkingen die vroeger onmogelijk waren.

Welke ontdekkingen zijn dat?
OREN: Een concreet voorbeeld is de bestrijding van geneesmiddelenresistente tuberculose, een ziekte die jaarlijks nog steeds 1,5 miljoen levens eist. Net zoals bij het coronavirus bestaan er verschillende varianten van de tuberculosebacterie. Er bestaan zeven soorten antibiotica om tuberculose te behandelen, maar bij sommige patiënten werken die niet meer. Dat is problematisch, want we zien nu al bacteriestammen die zelfs resistent zijn tegen de nieuwste antibiotica.
Dat resistentiemechanisme begrijpen is complex. We zien niet altijd een directe link tussen de antibiotica en de genetische mutaties van de bacteriestam die verantwoordelijk zijn voor de resistentie. Door verschillende datalagen van hetzelfde staal te combineren, proberen we die verborgen verbanden bloot te leggen.
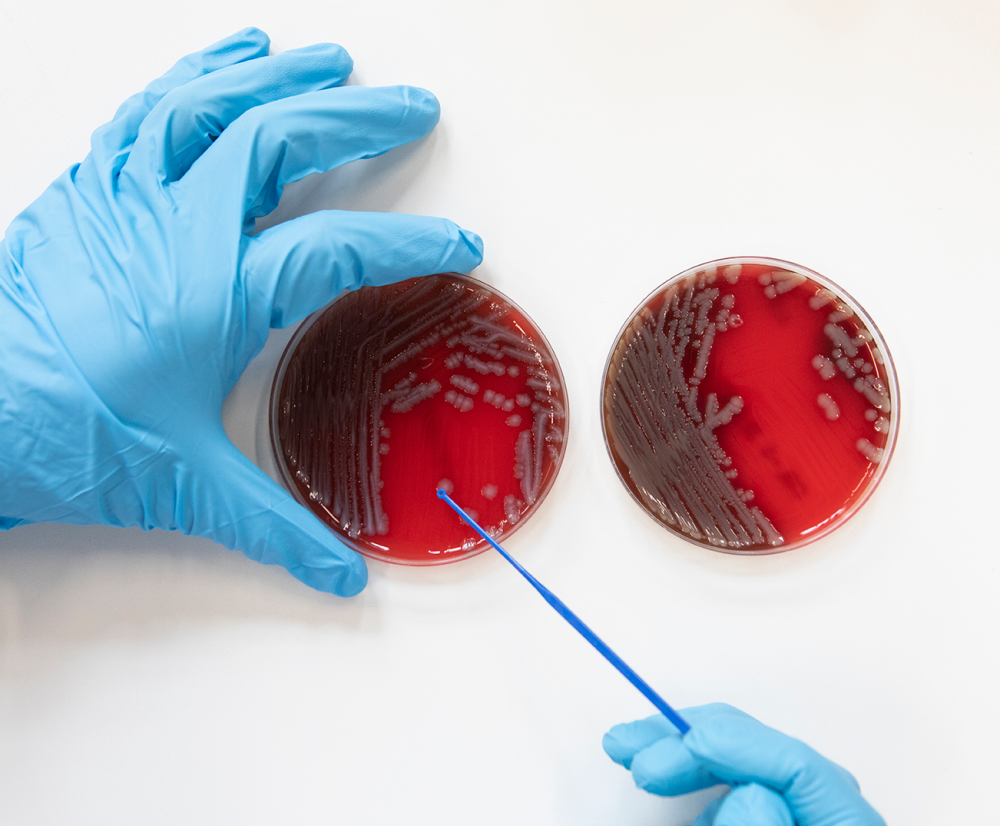
Hoe helpt AI daarbij?
OREN: We voeden een AI-model met alle beschikbare informatie: van wetenschappelijke publicaties tot experimentele resultaten en andere relevante data. Zo hopen we verbanden te vinden tussen resistente bacteriestammen en antibiotica die we anders niet zouden opmerken. Misschien helpt AI ons te begrijpen waarom resistentie ontstaat.
Daarnaast versnelt AI het onderzoeksproces enorm. Normaal duurt het zes tot zeven weken om te bepalen of een staal resistent is, omdat de bacterie moet worden opgekweekt. Met AI kunnen we voortdurend microscopische beelden nemen van de groei van de bacterie. Het model analyseert de groeipatronen en kan na enkele uren al resistentie voorspellen - lang voordat het zichtbaar is met het blote oog. Dat is een sterk voorbeeld van hoe AI onderzoek kan versterken.
Natuurlijk blijft menselijke controle cruciaal om AI-resultaten te verifiëren. We mogen niet vergeten: AI geeft ons superkrachten, maar ook superverantwoordelijkheden.

Wat zou u zeggen tegen collega’s die nog twijfelen over AI?
OREN: Ik hoop dat onderzoekers niet terugdeinzen voor AI en nieuwe technologieën. Eerlijk gezegd denk ik dat dit de nieuwe standaard wordt in de wetenschap, dus het is beter om mee te evolueren. Iedereen zal deze superkrachten krijgen.
Onze studenten zijn daar het bewijs van. Biologiestudenten moeten leren programmeren, en programmeurs hun biologie bijspijkeren. Vroeger duurde het bijna tien maanden om studenten op te leiden tot het gewenste niveau, nu kunnen ze vanaf dag één meedraaien. AI kan code schrijven of snel samenvattingen van recente literatuur geven. Het verandert werkelijk elk aspect van ons werk.
Zijn er ook grenzen aan deze technologieën?
OREN: Zeker. Omics en AI zijn geen wondermiddelen. Ze werken pas echt als ze worden gecombineerd met sterke lokale partnerschappen in het Globale Zuiden. Technologie helpt ons betere vragen te stellen, slimmere oplossingen te bedenken en precisiegeneeskunde dichter bij de mensen te brengen die ze het meest nodig hebben. Maar technologie alleen herstelt geen zwakke gezondheidssystemen. De echte innovatie zit in het koppelen van nieuwe tools aan gelijkheid, lokaal eigenaarschap en duurzame integratie.
Als technologie zomaar ‘gedropt’ wordt in lokale contexten, is dat alsof je iemand een Ferrari geeft zonder brandstof. Indrukwekkend, maar kan die daarmee doen? Daarom ontwikkelen we samen met lokale wetenschappers bio-informatica-opleidingen en dataplatformen, zodat zij zelfstandig omics kunnen toepassen en hun eigen volksgezondheidsbeleid kunnen vormgeven.
Spread the word! Deel dit artikel op